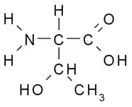
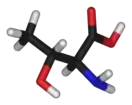
Треонин
Треони́н (англ. Threonine; α-амино-β-гидроксимасляная кислота; 2-амино-3-гидроксибутановая кислота) — гидроксиаминокислота; молекула содержит два хиральных центра, что обусловливает существование четырёх оптических изомеров: L- и D-треонина (3D), а также L- и D-аллотреонина (3L).
| Треонин | |||
|---|---|---|---|
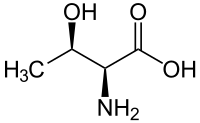 | |||
| Общие | |||
| Систематическое наименование |
2-амино-3- гидроксибутановая кислота |
||
| Сокращения |
Тре, Thr, T ACU,ACC,ACA,ACG |
||
| Хим. формула | HO2CCH(NH2)CH(OH)CH3 | ||
| Рац. формула | C4H9NO3 | ||
| Физические свойства | |||
| Молярная масса | 119,12 г/моль | ||
| Термические свойства | |||
| Температура | |||
| • плавления | 256 °C | ||
| Химические свойства | |||
| Константа диссоциации кислоты |
2,20 9,96 |
||
| Изоэлектрическая точка | 5,60 | ||
| Классификация | |||
| Рег. номер CAS | [72-19-5] | ||
| PubChem | 6288 | ||
| Рег. номер EINECS | 200-774-1 | ||
| SMILES | |||
| InChI | |||
| ChEBI | 16857 | ||
| ChemSpider | 6051 | ||
| Приведены данные для стандартных условий (25 °C, 100 кПа), если не указано иное. | |||
L-треонин вместе с 19 другими протеиногенными аминокислотами участвует в образовании природных белков. Для человека треонин является незаменимой аминокислотой. У бактерий, дрожжей и растений из L-треонина при участии фермента треониндезаминазы синтезируется другая незаменимая аминокислота изолейцин.
Суточная потребность в треонине для взрослого человека составляет 0,5 г, для детей — около 3 г.
Бактериями и растениями треонин синтезируется из аспарагиновой кислоты через стадию образования гомосерин-O-фосфата. Треонин участвует в синтезе коллагена и эластина, в белковом и жировом обмене, стимулирует иммунитет и помогает работе печени, препятствуя отложению в ней жиров.
Литература
- Химическая энциклопедия / Редкол.: Кнунянц И.Л. и др.. — М.: Советская энциклопедия, 1995. — Т. 4 (Пол-Три). — 639 с. — ISBN 5-82270-092-4.