Оксид хлора(VII)
Окси́д хло́ра(VII) (дихлорогептаоксид) Cl2O7,
(хлорный ангидрид) — кислотный оксид. Высший оксид хлора, в котором он проявляет степень окисления +7.
| Оксид хлора(VII) | |
|---|---|
 | |
| Общие | |
| Систематическое наименование |
Оксид хлора(VII) |
| Хим. формула | Cl2O7 |
| Рац. формула | Cl2O7 |
| Физические свойства | |
| Состояние | жидкость |
| Молярная масса | 182.901 г/моль |
| Плотность | 1,9 г/см³ |
| Термические свойства | |
| Температура | |
| • плавления | −91,5 °C |
| • кипения | 82 °C |
| • разложения | 120 °C |
| Энтальпия | |
| • образования | 251,0 кДж/моль |
| Классификация | |
| Рег. номер CAS | [12015-53-1] |
| PubChem | 123272 |
| SMILES | |
| InChI | |
| ChEBI | 52356 |
| ChemSpider | 109884 |
| Безопасность | |
| Пиктограммы ECB |
|
| NFPA 704 | |
| Приведены данные для стандартных условий (25 °C, 100 кПа), если не указано иное. | |
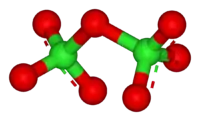
Молекула Cl2O7 имеет строение О3Cl—О—ClO3 (dCl—О = 0,1709 нм, в группах ClО3 — 0,1405 нм, угол ClOCl = 118,6°, ОClO 115,2°) c пространственной симметрией C2, молекула полярна (μ = 2,40⋅10−30 Кл·м).
Химические Свойства
Хлорный ангидрид представляет собой бесцветную маслянистую ядовитую жидкость. Cl2O7 взрывается при нагревании выше 120 °C и от удара, однако он более устойчив, чем оксид и диоксид хлора. Жидкий Cl2О7 устойчив до 60—70 °C, но примесь низших оксидов хлора существенно ускоряет его распад:
- ΔH = 135 кДж/моль
Медленно растворяется в холодной воде, образуя хлорную кислоту:
Хлорный ангидрид является сильным окислителем. Может вызвать самовоспламенение горючих веществ.
Получение
Получают Cl2О7 при осторожном нагревании хлорной кислоты с фосфорным ангидридом или олеумом:
Оксид хлора(VII) получают также электролизом раствора НClО4 на платиновых электродах ниже 0 °C (Cl2O7 накапливается в анодном пространстве). Чистый Cl2O7 можно синтезировать также при нагревании в вакууме некоторых перхлоратов, например, Nb(ClO4)5 или МоО2(ClO4)2.
Литература
- Реми Г. «Курс неорганической химии» М.: Иностранная литература, 1963
