Пентаналь
Пентаналь (также называемый амиловым альдегидом или валериановым альдегидом) — это альдегид, молекулярная формула которого .
| Пентаналь | |
|---|---|
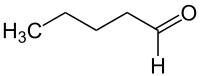 | |
| Общие | |
| Хим. формула | C5H10O |
| Физические свойства | |
| Плотность | 0,81 ± 0,01 г/см³[1] |
| Энергия ионизации | 9,82 ± 0,01 эВ[1] |
| Термические свойства | |
| Температура | |
| • плавления | −133 ± 1 ℉[1] и −92 °C[2] |
| • кипения | 217 ± 1 ℉[1] |
| • вспышки | 54 ± 1 ℉[1] |
| Давление пара | 26 ± 1 мм рт.ст.[1] |
| Классификация | |
| Рег. номер CAS | 110-62-3 |
| PubChem | 8063 |
| Рег. номер EINECS | 203-784-4 |
| SMILES | |
| InChI | |
| RTECS | YV3600000 |
| ChEBI | 84069 |
| ChemSpider | 7772 |
| Приведены данные для стандартных условий (25 °C, 100 кПа), если не указано иное. | |
Физические свойства
Бесцветная летучая легкокипящая жидкость с сильным, резким запахом. Поскольку в молекулах карбонильных соединений водородных связей нет, то температура кипения у них будет значительно ниже, чем у соответствующих спиртов. В пентанале она будет равна 103°С. Мало растворим в воде и хорошо растворим в органических растворителях (этанол, эфир…).
Химические свойства
Молярная масса=86,13.
Для пентаналя характерны:
- реакции нуклеофильного присоединения
- Присоединение циановодородной кислоты
- Присоединение гидросульфитов
- Взаимодействие со спиртами
- Гидратация
- Присоединение реактивов Гриньяра
- Реакции полимеризации
- Реакции полдиконденсации
- Окисление аммиачным раствором оксида серебра(реакция серебряного зеркала)
- Окисление гидрооксидом меди
- Реакция Канниццаро
- Галогенирование
- Гидрирование: пентаналь способен присоединять водород, восстанавливаясь до пентанола.
- Горение
Получение
Чаще всего пентаналь получают окислением пентанола оксидом меди, но также возможны и другие варианты.
Применение
Используется для получения пластмасс, конструкционного пластика, ароматизаторов.Так же используется в медицине и ароматизации .
Примечания
Литература
- Дерябина Н.Е. Органическая химия. Книга 1. Углеводороды и их монофункциональные производные. — 2012.
- Глинка Н.Л. Общая химия. — 2010.
This article is issued from Wikipedia. The text is licensed under Creative Commons - Attribution - Sharealike. Additional terms may apply for the media files.